引言 呼吸机出口有怎样的流程?小编为大家整理了一份指南。
近期,关于呼吸机出口的话题讨论度很高,呼吸机出口的相关问题,许多媒体也都进行了报道。那呼吸机出口有怎样的流程?小编为大家整理了一份指南。
一、产品分类
目前,我国未出台统一广泛使用的呼吸机分类标准。通常按照用途,呼吸机可分为成人、婴儿和新生儿、辅助呼吸和治疗用、麻醉、携带式急救和高频正压等六类。按照连接方式,可分为有创和无创两类。按照应用环境,可分为医用和家庭用两类。
近期出口欧盟、美国的多为用于成人、辅助呼吸和治疗、麻醉等用途的医用呼吸机。
二、出口资质
1.营业执照(经营范围有相关经营内容)。
2.企业生产许可证(生产企业)。
3.产品检验报告(生产企业)。
4.医疗器械注册证。
5.产品说明书(跟着产品提供)、标签(随附产品提供)。
6.产品批次/号(外包装)。
7.产品质量安全书或合格证(跟着产品提供)。
8.产品样品图片及外包装图片。
9.贸易公司须取得海关收发货人注册备案。
生产企业有进出口权,可以自行出口,如没有进出口权,可以通过外贸代理进行出口销售。
三、出口通关要求

关联提示:
自3月11日起,美国取消部分医疗物资进口关税,其中包括呼吸机。
禁限管理:
商务部 海关总署 国家药品监督管理局2020年第5号《关于有序开展医疗物资出口的公告》:自4月1日起,出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计的企业向海关报关时,须提供书面或电子声明,承诺出口产品已取得我国医疗器械产品注册证书,符合进口国(地区)的质量标准要求。海关凭药品监督管理部门批准的医疗器械产品注册证书验放。
四、出口退税
呼吸机及其零件、附件的出口退税率为13%。
五、各国准入条件
1. 美国
出口美国需FDA注册。国外的医疗器械必须指定一位美国代理人,该代理人负责紧急情况和日常事务交流。
2. 欧盟
出口欧盟需获得FSC(自由销售证书),该证书由唯一被欧盟指令授权的资质机构——欧洲经济区(EEA)的医疗器械主管机关出具。如企业产品已经获得CE标志,并已进行相关注册,出口欧盟不需要FSC,但出口欧洲经济区内其他非欧盟国家的,需提供FSC。
3. 日本
出口日本需PMDA注册。国外制造商必须向PMDA注册制造商信息。日本医药品和医疗器械综合机构(PMDA)。
4. 韩国
出口韩国需韩国卫生福利部下属食品药品安全部KFDA注册。韩国药监局Korea Pharmaceutical Traders Association韩国卫生福利部负责食品、药品、化妆品和医疗器械管理,下属食品药品安全部负责医疗器械管理。
5. 澳大利亚
出口澳大利亚需卫生部下属治疗商品管理局TGA注册。澳大利亚产品分类与欧盟基本一致,如企业产品已经获得CE标志,可以简化TGA注册程
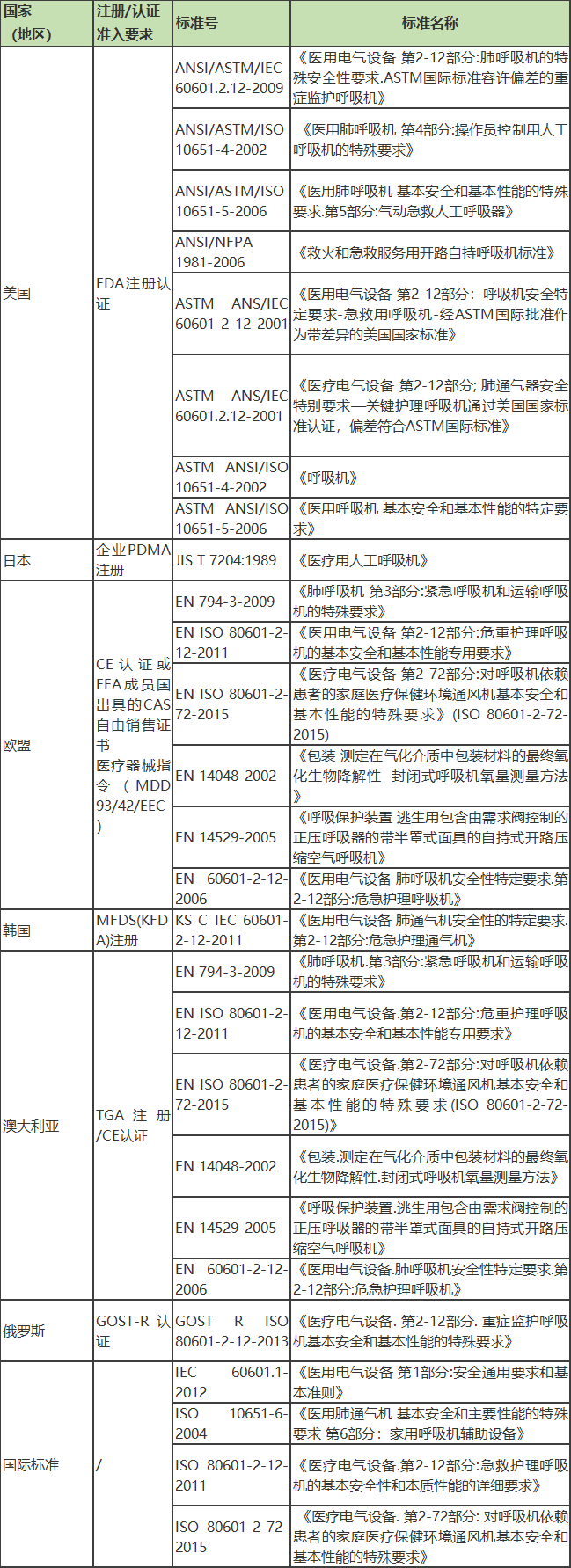
六、主要出口国家(地区)注册认证准入要求和检测标准

扫码关注二维码
2025-03-28 11:42
2025-03-30 12:11
2025-03-27 18:37
2025-04-02 12:00
2025-04-02 18:06
2025-03-31 10:33
扫码加入社群

扫一扫
关注亿恩公众号
